一、神经-骨骼肌接头处的兴奋传递
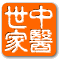
运动神经纤维在到达神经末梢处时先失去髓鞘,以裸露的轴突末梢嵌入到肌细胞膜上称作终板的膜凹陷中,但轴突末梢的膜和终板膜并不直接接触,而是被充满了细胞外液的接头间隙隔开,其中尚含有成分不明的基质;有时神经末梢下方的终板膜还有规则地再向细胞内凹入,形成许多皱褶,其意义可能在于增加接头后膜的面积,使它可以容纳较多数目的蛋白质分子,它们最初被称为N-型乙酰胆碱受体,现已证明它们是一些化学门控通道,具有能与ACh特异性结合的亚单位。在轴突末梢的轴浆中,除了有许多线粒体外还含有大量直径约50nm的无特殊构造的囊泡(图2-19)。用组织化学的方法可以证明,囊泡内含有ACh;此ACh首先在轴浆中合成,然后贮存在囊泡内。据测定,每个囊泡中贮存的ACh量通常是相当恒定的,且当它们被释放时,也是通过出胞作用,以囊泡为单位“倾囊”释放,被称为量子式释放。在神经末梢处于安静状态时,一般只有少数囊泡随机地进行释放,不能对肌细胞产生显著影响。但当神经末梢处有神经冲动传来时,在动作电位造成的局部膜去极化的影响下,大量囊泡向轴突膜的内侧面靠近,通过囊泡膜与轴突膜的融合,并在融合处出现裂口,使囊泡中的ACh全部进入接头间隙。据推算,一次动作电位的到达,能使大约200~300个囊泡的内容排放,使近107个ACh分子被释放。轴突末梢处的电位变化引起囊泡排放的过程十分复杂,但首先是轴突末梢膜的去极化,引起了该处特有的电压门控式Ca2+通道开放,引起细胞间隙液中的Ca2+进入轴突末梢,触发了囊泡移动以至排放的过程。Ca2+的进入量似乎决定着囊泡释放的数目;细胞外液中低Ca2+或(和)高Mg2+,都可阻碍ACh的释放而影响神经-肌接头的正常功能。已故冯德培院士在30年代对神经-肌接头的化学性质传递进行过重要的研究。
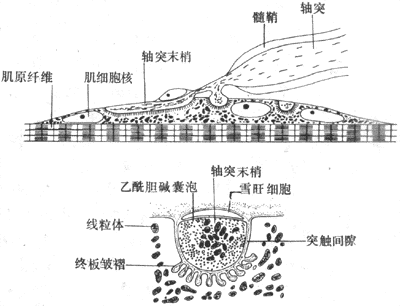
图2-19 神经-肌接头处的超微结构示意图
当ACh分子通过接头间隙到达终板膜表面时,立即同集中存在于该处的特殊通道蛋白质的两个α-亚单位结合,每分子的通道将结合两个分子的ACh,由此引起的蛋白质分子内部构象的变化会导致它的通道结构的开放。这种通道开放时,孔道的横截面比前面提到的Na+通道的面积为大,可允许Na+、K+甚至少量Ca2+同时通过;由于这几种离子正常时在膜内处的分布特点,实际出现的是Na+的内流和K+的外流,其总的结果是使终板膜处原有静息电位减小,向零值靠近,亦即出现膜的去极化;这一电变化,称为终板电位,它的出现约较神经冲动到达接头前膜处晚0.5~1.0ms。有人曾在运动神经无冲动到达末梢时,记录到由于个别囊泡的自发释放在终板膜上引起的微小的电变化,称为微终板电位。终板电位与前述的局部兴奋电反应有类似的性质:不表现“全或无”特性,其大小与接头前膜释放的ACh的量成比例;无不应期,可表现总和现象等,如我们一般记录到的终板电位就是多数微终板电位总和的结果。终板电位产生时,它将以电紧张性扩布的形式影响终板膜周围一般肌细胞膜。一般的肌细胞膜与神经轴突的膜性质类似,其中主要含电压门控式Na+通道和K+通道;因而当同终板膜邻接的肌细胞膜的静息电位由于终板电位的影响而去极化到该处膜的阈电位水平时,就会引发一次向整个肌细胞膜作“全或无”式传导的动作电位,后者再通过所谓“兴奋-收缩耦联”,引起肌细胞出现一次机械收缩。
正常情况下,一次神经冲动所释放的ACh以及它所引起的终板电位的大小,大约超过引起肌细胞膜动作电位所需阈值的3~4倍,因此神经肌接头处的兴奋传递通常是1对1的,亦即运动纤维每有一次神经冲动到达末梢,都能“可靠地”使肌细胞兴奋一次,诱发一次收缩;这一点与将来要讲的神经元之间的兴奋传递有明显不同(见第十章)。接头传递能保持1对1的关系,还要靠每一次神经冲动所释放的ACh能够在它引起一次肌肉兴奋后被迅速清除,否则它将持续作用于终板而使终板膜持续去极化,并影响下次到来的神经冲动的效应。已知,ACh的清除主要靠胆硷酯酶的降解作用来完成,此酶主要分布在接头间隙中和接头后膜上,它们大约可以在2.0ms的时间内将一次神经冲动所释放的ACh清除掉。许多药物可以作用于接头传递过程中的不同阶段,影响正常的接头功能。例如,美洲箭毒和α-银环蛇毒可以同ACh竞争终板膜的ACh受体亚单位,因而可以阻断接头传递而使肌肉失去收缩能力;有类似作用的药物称为肌肉松弛剂;有机磷农药和新斯的明对胆碱酯酶有选择性的抑制作用,可造成ACh在接头和其他部位的大量积聚,引起种种中毒症状。重症肌无力是由于体内骨骼肌终板处的ACh门控通道数量不足或功能障碍所引起。
二、骨骼肌细胞的微细结构
骨骼肌细胞在结构上最突出之点,是含有大量的肌原纤维和丰富的肌管系统,且其排列高度规则有序。肌细胞是体内耗能作功,完成机体多种机械运动的功能单位。
(一)肌原纤维和肌小节
每个肌纤维含有大量直径1~2μm的纤维状结构,称为肌原纤维,它们平行排列,纵贯肌纤维全长,在一个细胞中可达上千条之多(图2-20)。每条肌原纤维的全长都呈现规则的明、暗交替,分别称为明带和暗带;而且在平行的各肌原纤维之间,明带和暗带又都分布在同一水平上;暗带的长度比较固定,不论肌肉处于静止、受到被动牵拉或进行收缩时,它都保持1.5μm的长度;在暗带中央,有一段相对透明的区域,称为H带,它的长度随肌肉所处状态的不同而有变化;在H带中央亦即整个暗带的中央,又有一条横向的暗线,称为M线。明带的长度是可变的,它在肌肉安静时较长,并且在一定范围内可因肌肉所受的被牵引而变长;但明带在肌肉收缩时可变短。明带中央也有一条横向的暗线,称为z线(或z盘)。目前已经肯定,肌原纤维上每一段位于两条z线之间的区域,是肌肉收缩和舒张的最基本单位,它包含一个位于中间部分的暗带和两侧各1/2的明带,合称为肌小节(sarcomere)。由于明带的长度可变,肌小节的长度在不同情况下可变动于1.5~3.5μm之间;通常在体骨骼肌安静时肌小节的长度约为2.0~2.2μm。
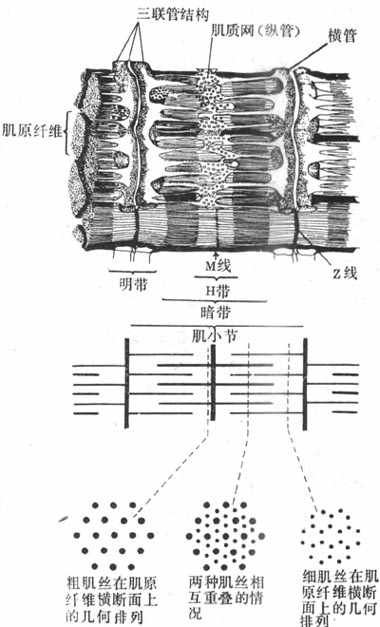
图2-20 骨骼肌细胞的肌原纤维和肌管系统
注意肌小节能的组成和不同部位肌小节横断布粗、细肌丝的几何排列
用X-线衍射等更精密的方法进一步发现,肌小节的明带和暗带包含有更细的、平行排列的丝状结构,称为肌丝。暗带中含有的肌丝较粗,直径约10nm,称为粗肌丝,其长度与暗带相同;实际上暗带的形成就是由于粗肌丝的存在,M线则是把成束的粗肌丝固定在一定位置的某种结构。明带中的肌丝较细,直径约5nm,称为细肌丝;它们由z线结构向两侧明带伸出,每侧的长度都是1.0nm,它的游离端在肌小节总长度小于3.5nm的情况下,必然有一段要伸入暗带,和粗肌丝处于交错和重叠的状态;如果由两侧z线伸入暗带的细肌丝未能相遇而隔有一段距离,这就形成了H带。肌肉被拉长时,肌小节长度增大,这时细肌丝由暗带重叠区拉出,使明带长度增大,H带也相应地增大(图2-20,下)。
粗、细肌丝相互重叠时,在空间上也呈现规则排列,这可从肌原纤维的横断面上看出。图2-20下方表示在肌小节的不同位置将肌原纤维横节时,断面上所能看到的两种肌丝的分布情况。在通过明带的横断面上只有细肌丝,它们的所在位置相当于一个正六边形的各顶点;在通过H带的横断面上只有粗肌丝,它们都处于正三边形的各顶点上;而在H带两侧的暗带的横断面上,则可看到粗、细肌丝交错存在的情况,这里,每一条粗肌丝正处在以六条细肌丝为顶点的正六边形的中央,而这就为收缩时粗细肌丝之间的相互作用准备了条件。
(二)肌管系统
肌管系统指包绕在每一条肌原纤维周围的膜性囊管状结构,由来源和功能都不相同的两组独立的管道系统组成。一部分肌管的走行方向和肌原纤维相垂直,称为横管系统或称T管,是由肌细胞的表面膜向内凹入而形成;它们穿行在肌原纤维之间,并在z线水平(有些动物是在暗带和明带衔接处的水平)形成环绕肌原纤维的管道;它们相互交通,管腔通过肌膜凹入处的小孔与细胞外液相通。将标记物加入到细胞的浸浴液中,这些物质可以很快在每一条环绕肌小节的横管系统中出现,但不能进入肌浆和肌浆网中去。肌原纤维周围还有另一组肌管系统,就是肌浆网,它们的走行方向和肌小节平行,称为纵管系统或称为L管;纵管系统或肌浆网主要包绕每个肌小节的中间部分,这是一些相互沟通的管道,但是在接近肌小节两端的横管时管腔出现膨大,称为终末池,它使纵管以较大的面积和横管相靠近。每一横管和来自两侧肌小节的纵管终末池,构成了三联管结构(图2-20,上)。据研究,横管和纵管的膜在三联管结构处并不接触,中间尚隔有约12nm的间隙,说明两组管道的内腔并不直接沟通,但这样的结构显然有利于细胞内外之间某种形式的信息传递。目前普遍承认的看法是,横管系统的作用是将肌细胞兴奋时出现在细胞膜上的电变化沿T管膜传入细胞内部,肌浆网和终末池的作用是通过对钙离子的贮存、释放和再积聚,触发肌小节的收缩和舒张;而三联管结构是把肌细胞膜的电变化和细胞内的收缩过程衔接或耦联起来的关键部位。
三、骨骼肌的收缩机制和兴奋-收缩耦联
Huxley等在50年代初期就提出了用肌小节中粗、细肌丝的相互滑行来说明肌肉收缩的机制。这一被称为滑行理论(sliding theory)的主要内容是:肌肉收缩时虽然在外观上可以看到整个肌肉或肌纤维的缩短,但在肌细胞内并无肌丝或它们所含的分子结构的缩短,而只是在每一个肌小节内发生了细肌丝向粗肌比之间的滑行,亦即由z线发出的细肌丝在某种力量的作用下主动向暗带中央移动,结果各相邻的z线都互相靠近,肌小节长度变短,造成整个肌原纤维、肌细胞乃至整条肌肉长度的缩短。滑行现象最直接的证明是,肌肉收缩时并无暗带长度的变化,而只能看到明带长度的缩短;并且与此同时也看到暗带中央H带相应地变窄。这只能说明,细肌丝在肌肉收缩时也没有缩短,只是它们更向暗带中央移动,和粗肌丝发生了更大程度的重叠。这种变化只能用粗、细肌丝之间出现了相对运动即滑行现象来解释。滑行理论需要进一步说明的问题是:肌肉收缩时究竟是什么力量促使细肌丝向粗肌丝之间滑行,以及怎样把这些过程和肌肉膜的兴奋过程联系起来。近年来,由于肌肉生物化学及其他细胞生物学技术的发展,肌丝滑行的机制已基本上从组成肌丝的蛋白质分子结构的水平得到阐明,对于与滑行的开始和终止有关的各种控制因素,也有了较较深入的了解。
(一)肌丝的分子组成和横桥的运动
滑行现象的引起与组成肌丝的蛋白质分子结构和它们的特性有直接的关系。粗肌丝主要由肌凝蛋白(亦称肌球蛋白)所组成,它们的分子在粗肌丝中呈独特的有规则的排列。一条粗肌丝大约含有200~300个肌凝蛋白分子,每个分子长150nm,呈长杆状而在一端有球状膨大部。在组成粗肌丝时,各杆状部朝向M线而聚合成束,形成粗肌丝的主干,球状部则有规则地裸露在M线两侧的粗肌丝主干的表面,形成横桥(图2-21,左)。当肌肉安静时,横桥与主干的方向相垂直,由粗肌丝表面突出约6nm。用X-线衍射法证明,横桥在粗肌丝表面的分布位置也是严格有规则的,即在粗肌丝的同一周径上只能有两个相隔180°的横桥突出;在与此周径相隔14.3nm的主干上又有一对横桥突出,但与前一对有60°的夹角;如此反复,到第四对横桥出现时,其方向正好与第一对横桥相平行,且与第一对横桥相隔42.9nm(图示-21,右)。上述横桥的分布情况,正好与一条粗肌丝为6条细肌丝所环绕的情况相对应,亦即在所有横桥出现的位置,正好有一条细肌丝与之相对;而对于每条细肌丝来说,粗肌丝表面每隔42.9nm就伸出一个横桥与之相对(图2-21)。这种对应关系,对于粗、细肌丝之间的相互作用显然是十分有利的。
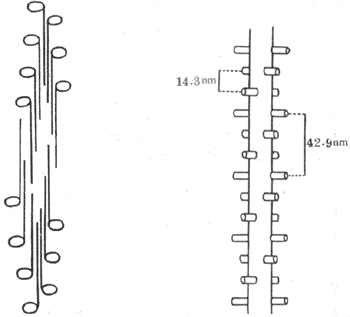
图2-21 粗肌丝中肌凝蛋白分子的排列示意图
左、肌凝蛋白分子的长杆状部横向聚合,形成粗肌丝主干,球状部裸露在表面,形成横桥
右、横桥在粗肌丝表面的几何排列
现已证明,横桥所具有的生物化学特性对于肌丝的滑行有重要意义。横桥的主要特性有二:一是横桥在一定条件下可以和细肌丝上的肌纤蛋白分子呈可逆性的结合,同时出现横桥向M线方向的扭动,继而出现横桥和细肌丝的解离、复位,然后再同细肌丝上另外的点结合,出现新的扭动,如此反复,使细肌丝继续向M线方向移动;二是横桥具有ATP酶的作用,可以分解ATP而获得能量,作为横桥摆动和作功的能量来源。由此可见,横桥和细肌丝的相互作用,是引起肌丝滑行的必要条件。
细肌丝至少由三种蛋白质组成,其中60%是肌纤蛋白(亦称肌动蛋白)。肌纤蛋白与肌丝滑行有直接的关系,故和肌凝蛋白一同被称为收缩蛋白质。肌纤蛋白分子单体呈球状,但它们在细肌丝中聚合成双螺旋状,成为细肌丝的主干(图2-22)。细肌丝中另外有两种蛋白质,它们不直接参与肌丝间的相互作用,但可影响和控制收缩蛋白质之间的相互作用,故称为调节蛋白质;其中一种是原肌凝蛋白,也呈双螺旋结构,在细肌丝中和肌纤蛋白双螺旋并行,但在肌肉安静时原肌凝蛋白的位置正好在肌纤蛋白和横桥之间(图2-23,左)这就起了阻碍两者相互结合的作用;另一种调节蛋白质称为肌钙蛋白(亦称原宁蛋白),肌钙蛋白在细肌丝上不直接和肌纤蛋白分子相连接,而只是以一定的间隔出现在原肌凝蛋白的双螺旋结构之上。肌钙蛋白的分子呈球形,含有三个亚单位(图2-22):亚单位C中有一些带双负电荷的结合位点,因而对肌浆中出现的Ca2+(以及其他可能出现的两价正离子和H+)有很大的亲和力;亚单位T作用是把整个肌钙蛋白分子结合于原肌凝蛋白;而亚单位I的作用是在亚单位C与Ca2+结合时,把信息传递给原肌凝蛋白,引起后者的分子构象发生改变,解除它对肌纤蛋白和横桥相互结合的阻碍作用。
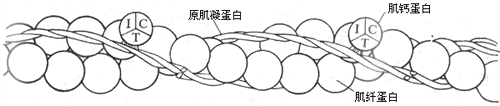
图 2-22 细肌丝的分子组成
I、T、C分别代表肌钙蛋白的三个亚单位
肌丝滑行的基本过程一般公认为:当肌细胞上的动作电位引起肌浆中Ca2+浓度升高时,作为Ca2+受体的肌钙蛋白结合了足够数量的Ca2+,这就引起了肌钙蛋白分子构象的某些改变,这种改变“传递”给了原肌凝蛋白,使后者的构象也发生某些改变,其结果是使原肌凝蛋白的双螺旋结构发生了某种扭转,这就把安静时阻止肌纤蛋白和横桥相互结合的阻碍因素除去,出现了两者的结合。在横桥与肌纤蛋白的结合、扭动、解离和再结合、再扭动构成的横桥循环过程中,使细肌丝不断向暗带中央移动;与此相伴随的是ATP的分解消耗和化学能向机械能的转换,完成了肌肉的收缩(图示2-23)。
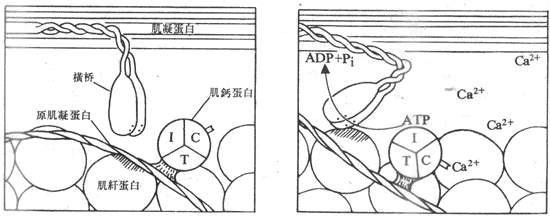
图2-23 Ca2+通过和肌钙蛋白的结合,诱发横桥和肌纤蛋白之间的相互作用
上述的横桥循环在一个肌小节以至整个肌肉中都是非同步地进行的,这样才可能使肌肉产生恒定的张力和连续的缩短。至于能参与循环的横桥数目以及横桥循环的进行速率,则是决定肌肉缩短程度、缩短速度以及所产生张力的关键因素,这将在分析肌肉收缩的力学表现时再作讨论。下面叙述正常条件下引发和终止横桥循环的肌浆中Ca2+浓度的突然升高和快速下降是怎样发生的。
(二)骨骼肌的兴奋-收缩耦联
在整体情况下,骨骼肌总是在支配它的躯体传出神经的兴奋冲动的影响下进行收缩的;直接用人工刺激作用无神经支配的骨骼肌,也可引起收缩。但不论何种情况,刺激在引起收缩之前,都是先在肌细胞膜上引起一个可传导的动作电位,然后才出现肌细胞的收缩反应。这样,在以膜的电变化为特征的兴奋过程和以肌丝的滑行为基础的收缩过程之间,必然存在着某种中介性过程把两者联系起来,这一过程,称为兴奋-收缩耦联。目前认为,它至少包括三个主要步骤:电兴奋通过横管系统传向肌细胞的深处;三联管结构处的信息传递;肌浆网(即纵管系统)对Ca2+释放和再聚积。
横管系统对正常肌细胞的兴奋-收缩耦联是十分必要的。用含有甘油的高渗任氏液浸泡肌肉一段时间,再把它放回到一般任氏液中,这样的处理可以选择性地破坏肌细胞的横管系统;这时如果再给肌肉以外加刺激,虽然仍可在完好的肌细胞膜上引起动作电位,但不再能引起细胞收缩。近年来证明,横管膜和一般肌细胞膜有类似的特性,又是后者的延续部分,因而它也可以产生以Na+内流为基础的膜的去极化甚或动作电位;当一般细胞膜因兴奋而产生动作电位时,这一电变化可沿着凹入细胞内部的横管膜传导,深入到三联管结构和每个肌小节的近旁。
实际测定还证明,肌肉安静时肌浆中的Ca2+浓度低于10-7mol/L,但在膜开始去极化的很短时间内,可以在1~5ms内升高到10-5mol/L的水平,亦即增高100倍之多。这样多的Ca2+由何而来?用放射性45Ca自显影等技术证明,肌肉安静时Ca2+主要停留和聚积在z线附近,相当于肌浆网的终末池部位;肌肉收缩时,Ca2+由这里向暗带区扩散,触发横桥循环。这样问题就归结为:当肌膜上的电变化沿横管系统到达三联管部分时,一定有某种因子把横管膜上发生的变化传递给了相距不远的肌浆网膜上的类似Ca2+通道的结构,引起后者分子的变构作用,使通道开放,于是肌浆网内高浓度的Ca2+就不需耗能而靠易化扩散进入肌浆,到达肌丝区。传递这一信号的因子,有人认为是横管膜上存在的一种特殊蛋白,平时对肌浆网Ca2+通道外侧开口有机械堵塞作用,但在横管膜有电变化时发生变构作用,使原来的堵塞作用解除;也有人认为横管膜可因电变化而产生了第二信使类物质IP3(见本章第二节),由后者作用于Ca2+通道使之开放。由于三联管外有关的膜和膜中蛋白质几乎可以相互接触,因而第一种控制形式还是有可能的。
释放到肌浆中的Ca2+怎样被迅速除去,目前已证明是由于肌浆网膜结构中存在的一种特殊的离子转运蛋白质即钙泵活动的结果。钙泵是一种Ca2+依赖式ATP酶,目前已被分离提纯,它占肌浆网膜蛋白质总量的60%;在肌浆中Ca2+增高情况上,它可以分解ATP获得能量,将Ca2+在逆浓度差的情况下由肌浆转运到肌浆网内腔中去;由于肌浆中Ca2+浓度的降低,和肌钙蛋白结合的Ca2+也解离,引起肌肉舒张。
四、骨骼肌收缩的外部表现和力学分析
骨骼肌在体内的功能,就是它们在受刺激时能产生缩短或(和)张力,藉以完成躯体的运动或(和)抵抗外力的作用。当肌肉克服某一外力而缩短,或肌肉因缩短而牵动某一负荷时,肌肉就完成了一定量的机械功,其数值等于它所克服的阻力(或负荷)和肌肉缩短长度的乘积;如以缩短速度乘以负荷,则得出肌肉的输出功率。但肌肉在收缩时究竟以产生张力为主或缩短为主,以及收缩时能作多少功,则要看肌肉收缩时所遇到的负荷条件和肌肉本身的功能状态。
肌肉在体内或实验条件下可能遇到的负荷主要有两种:一种是在肌肉收缩前就加在肌肉上的,如把一条肌肉顺着它的肌原纤维的走行方向悬挂起来而把上端固定,再在另一端悬挂一定数量的重物,后者就是前负荷。前负荷使肌肉在收缩前就处于某种程度的被拉长状态,使它具有一定的长度,这称为初长度;这样由于前负荷的不同,同一肌肉就要在不同的初长度条件下进行收缩。另一种负荷称为后负荷,它是在肌肉开始收缩时才能遇到的负荷或阻力,它不增加肌肉的初长度,但能阻碍收缩时肌肉的缩短。可以理解,对于某一具体的肌肉来说,实验中所加负荷、特别是前负荷不应当过大,因为后者在肌肉收缩前就可能因过度的牵拉而损伤肌肉本身的结构;至于后负荷,它在大到一定程度就足以抵抗肌肉收缩所产生的最大张力,因而肌肉不再表现缩短,出现等长收缩,亦即这时肌肉虽进行了收缩,并未有长度改变;在这种情况下继续增加后负荷,显然不会对肌肉的收缩有什么影响。
据上述,能影响肌肉收缩时作功能力或其力学表现的因素至少有三个,即前负荷、后负荷和肌肉本身的功能状态(即肌肉收缩能力)。要分析某一因素影响的最简单办法,就是使其他因素保持在某一恒定值而改变要观察因素的值,得到一组数据并作成一条座标曲线来进行分析。
(一)前负荷或肌肉初长度对肌肉收缩的影响枣长度-张力曲线
为了保持在实验过程中肌肉本身的功能状态基本保持不变,通常选用代谢速度较慢的两栖类如蛙腓肠或缝匠进行实验,实验布置如图2-24A所示。肌肉在下方被固定,并且边了一个灵敏的张力换能器来记录肌肉收缩前和收缩后的张力产生情况;肌肉的上方连一个可移动的按钮,可以上下移动而改变肌肉的初长度,但不论初长度固定在什么长度,同旋钮相连的固定杆是不能动的,这就意味着把后负荷固定在无限大时的位置,肌肉在收缩时不可能缩短而只能产生张力(即前面所说的等长收缩),于是就可以观察初长度不同时对同一肌肉所能产生张力的影响了。
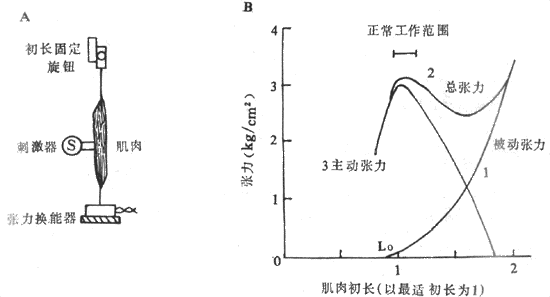
图2-24 肌肉初长度对肌肉收缩的影响
A:在实验布置中,下方是张力换能器,它位置固定,能把所受张力转变为相应的
电信号,上方旋钮可将肌肉初长在给肌肉刺激前固定于预定长度
B:3条曲线分别代表肌肉在初长度改变时的张力改变情况,被动张力指改变初长而尚未收缩的
肌肉的张力改变,总张力是在已有被动张力的基础上肌肉收缩时产生的主动张力与前者之和
图2-24B的长度-张力曲线反映了在依次改变肌肉的初长度时(横座标)在张力换能器上记录到的肌肉的张力产生的情况(纵座标)。曲线1是只改变肌肉初长度并不刺激肌肉收缩时肌肉所受的拉力,称为被动张力曲线,它反映安静肌肉具有某种弹性,在受到牵拉时产生某种回弹力,但牵拉超过某种程度,达到了弹性限度,被动张力急速增大,有可能造成组织损坏,其过程有如拉长一个弹簧时类似。曲线2是肌肉在具有不同前负荷即已具有被动张力的条件下进行一次收缩时记录到的张力变化,曲线的每一点都代表那个初长度时肌肉已有的被动张力和收缩时新产生的张力之和,故整个曲线称为总张力曲线;因此,由曲线2代表的不同初长度时的总张力减去同一初长度时的被动张力,就能得到曲线3,它表示肌肉在不同前负荷时进行收缩所能产生的张力,故称为主动张力曲线,它反映了本实验中要观察的内容,即不同前负荷或初长度对肌肉收缩所能产生的张力影响:当前负荷开始增加时,每次收缩所产生的主动张力也相应地增大,但在超过某一限度后,再增加前负荷反而使主动张力越来越小,以致于为零,如曲线3右端所示。这个结论也可以表达为,对于肌肉在等长度收缩条件下所产生的主动张力大小,存在着一个最适前负荷和与之相对应的最适初长度,相当于图2-24B横座标上Lo的位置,在这样的初长度情况下进行收缩,产生的张力最大。
肌肉在最适初长度条件下进行收缩何以能产生最大的张力,很容易根据肌肉被前负荷拉长时对每一肌小节中粗、细肌丝相互关系的改变来解释。已知,肌肉产生张力和缩短,靠的是粗肌丝表面的横桥和细肌丝之间的相互作用;肌肉初长度的大小,决定着每个肌小节的长度,亦即细肌丝和粗肌丝重叠的程度,而后者又决定于肌肉收缩时有多少横桥可以与附近的细肌丝相互作用。从理论上分析,粗肌丝的长度是1.5μm,但在M线两侧各为0.1μm的范围内正常时没有横桥,因此在M线两侧有横桥的粗肌丝长度各为0.65μm,这样当每侧细肌丝伸入暗带0.65μm(尚未于明带的细肌丝长度为0.35μm),亦即肌小节总长度为2.2μm时,粗肌丝上的每个横桥都能与细肌丝作用,因而收缩时能出现最佳的效果。当肌肉处于最适前负荷或最适初长度时,每个肌小节的长度正是2.2μm,如图2-25箭头3所示。如果稍稍减少前负荷使肌小节长度2.0μm(箭头2),尽管每侧细肌丝又多伸入暗带0.1μm(这时两侧细肌丝正好相遇),但这一段正是粗肌丝上无横桥伸出的部分,因而肌肉收缩时起作用的横桥数目并未增多(相当于图2-25中的箭头2)。至于再减小肌小节的长度,则细肌丝可能穿过M线或两侧肌丝相互重合和卷屈,因而造成收缩张力下降(图中箭头1)。反之,如果前负荷超过最适前负荷,收缩前肌小节的长度将大于2.2μm,细肌丝和粗肌丝相互重合的程度逐渐变小,使得肌肉收缩时起作用的横桥数也减少,造成所产生张力的下降;当前负荷使肌小节长度增加到3.5μm时,细肌丝将全部由暗带拉出,这时肌肉受刺激时不再产生主动张力(图中箭头4)。由此可见,通过前负荷对肌小节中粗、细肌丝重合程度的影响,可以说明骨骼肌长度-张力曲线的特点。
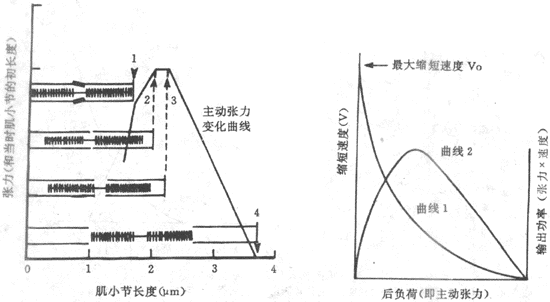
图2-25 不同初长度时粗、细肌丝重合程度和产生张力的关系示意图
用肌小节在不同前负荷时粗、细肌丝相对位置的改变,来说明不同前负荷时所产生的主动张力的不同:在箭头1所指的初长度时,每个肌小节中两侧细肌丝伸入暗带过多,互相重叠或发生卷屈,不利于与横桥间的相互作用;在箭头2和3所指的情况下,肌小节中全部横桥都可与细肌丝相互作用,产生出最大主动张力;在箭头4的情况下,细肌丝相互全部由暗带被拉出,失去产生张力的条件
图2-26 肌肉的张力-速度关系曲线
在肌肉前负荷固定在适当值的条件下,改变后负荷对肌肉产生张力(横座标)
和速短速度(左侧纵座标)相互关系的影响,这称为张力-速度关系曲线(曲线1),
由此曲线可以算出不同后负荷时的输出功率(右侧纵座标),组成了曲线2
(二)肌肉后负荷对肌肉收缩的影响-张力-速度曲线
据前述,如在实验室装置的设计中使一条骨骼肌的前负荷固定不变而可以人为地改变后负荷,即可观察不同后负荷对肌肉收缩的影响。一般情况下,可以把肌肉的前负荷固定在它的最适前负荷(这时出现的被动张力极小(见图2-24B),然后,在逐次改变后负荷的情况下观察肌肉收缩时的情况。不论在任何前负荷的情况下,如果所加后负荷超过了肌肉收缩时所能产生的最大张力(注意负荷的重量值和肌肉产生的张力的值可以用相同的物理单位度量,而且有相同的值),那么肌肉收缩时将只产生张力而不出现肌肉长度的改变。因此,在改变后负荷的实验中所加的后负荷都应小于这个最大张力,那么肌肉在收缩时产生的主动张力超过这个后负荷的值时,它将会出现一定程度的长度缩短,使移动酌相同的距离,并且由于后者也可以算出一个缩短速度来(可以是初速度或平均速度)。后负荷愈小,肌肉产生的张力将较早地超过这个负荷,并且出现较大的缩短长度和缩短速度,但相当于负荷值的肌肉张力却在缩短的过程中保持不变。这样就得到了改变后负荷时,肌肉产生张力和其缩短速度变化的关系曲线(为了计算输出功率,一般只分析缩短速度和张力的关系),即图2-26曲线1,称为张力-速度曲线。该曲线类似一条双曲线,横座标表示肌肉所产生的张力,纵座标表示收缩速度,双曲线的性质则说明这二者大致呈反比的关系,即后负荷减小时,使肌肉产生的张力减小,但可得到一个较大的缩短速度;在曲线同纵轴相交的点,说明后负荷理论上为零时,可以得到该肌肉在当时的功能状态下的最大收缩速度,在图2-26中用V表示;但这时因无负荷,肌肉并未作功,亦无功率输出。在曲线同横轴相交的点,后负荷的值相当于肌肉所能产生的最大张力,这时不能移动负荷,也没有作功和功率输出;在这两个极端之间,在不同的后负荷时都能看到肌肉在产生与负荷相同的张力的情况下使负荷移动一定距离,这种类型的收缩,称为待张收缩,都可作功和有功率输出,但以后负荷相当于最大张力的30%左右时,肌肉的输出功率最大,如图2-26中曲线2所示。
(三)肌肉收缩能力的改变对肌肉收缩的影响
上述的前、后负荷的改变对肌肉收缩时张力产生、缩短速度以及作功能力等力学表现的影响,显然是在肌肉功能状态恒定的情况下对所处负荷条件改变所作的不同反应。但肌肉的状态也是可以改变的,它也可以影响肌肉收缩的效率。例如,缺氧、酸中毒、肌肉中能源物质缺乏,以及其他原因引起的兴奋-收缩耦联、肌肉蛋白质或横桥功能特性的改变,都可能降低肌肉收缩的效果,而钙离子、咖啡因、肾上腺素等体液因素则可能通过影响肌肉的收缩机制而提高肌肉的收缩效果。将影响肌肉收缩效果的肌肉内部功能状态的改变,定义为肌肉收缩能力(contractility)的改变,以区别于肌肉收缩时外部条件即前、后负荷改变所导致的收缩效果的改变。这样的区分虽然在概念上比较容易,但在具体情况下要区分哪些改变是由于肌肉收缩能力的改变所引起,哪些是由于负荷条件的改变所引起,常常十分困难。例如,一个肌肉的最大张力变大了,可能是由于肌肉收缩能力的提高,但也可能是由于在这次收缩前它处于最适初长度;一个肌肉等张收缩时的收缩速度增大了,可能是由于后负荷的减小,也可能是它处于最适初长,但也可能是由于肌肉收缩能力的提高,或三者兼而有之。这就是说,很难简单地根据肌肉某项力学指标的改变,确定是否发生了肌肉收缩能力的改变。从理论上讲,肌肉收缩能力的改变对肌肉收缩的各力学表现的影响是“非选择性”的,即收缩能力的提高可使图2-24B中的长度-张力曲线(主动张力)和图2-26中的张力-速度曲线的位置都升高。显然,为了检查收缩能力是否改变而再绘制一条条座标曲线是十分复杂的;为了简便,如果能让同一肌肉所处的前、后负荷条件不变而发现有肌肉收缩速度的改变,或使肌肉维持最适初长度而有最大张力的改变,则都表示肌肉收缩能力发生了改变;因为在这些条件下可以肯定,这些收缩效果的改变并不是由于前、后负荷的改变所引起,因而只能是由于肌肉的内在性能的改变引起的。
(四)肌肉的单收缩和单收缩的复合
整块骨骼肌或单个肌细胞受到一次短促的刺激时,先是产生一次动作电位,紧接着出现一次机械收缩,后者称为单收缩;根据收缩时肌肉所处的负荷条件不同,单收缩可以是等长的,也可以是等张的。前面叙述的肌肉收缩时各种力学表现,就是以单收缩为观察对象而进行分析的。但在正常体内,当骨骼肌在运动神经的支配下进行自然收缩时,几乎是无例外地接受来自神经的连续刺激,因此有必要进一步分析肌肉有受到不同频率的连续刺激时可能发生的情况。为了便于分析,先观察一下肌肉单收缩时电变化和机械变化在时间上的关系。图2-27是猫胫前有一次等长单收缩时张力变化的全过程,同时记录了肌肉的动作电位。注意图中电反应的开始要较张力增加的开始为早,而且电变化在张力达到顶点以前早已结束;以张力最高点为界,收缩全过程可分为收缩期和舒张期,前者持续时间较后者为短。整个单收缩的时间因肌肉不同而有显著差异,如人的眼外肌的一次单收缩不超过10ms,而腓肠肌可达100ms以上。
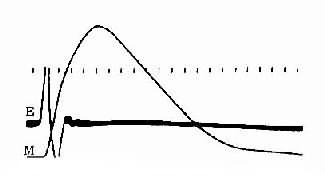
图2-27 猫胫前肌的等长单收缩曲线
M:肌肉收缩时的张力变化曲线
E:肌肉的双相动作电位记录时标每 格相当于0.01s
如果给肌肉以连续的脉刺激,肌肉的收缩情况将随刺激的频率而有不同。如图2-28所示,在刺激的频率较低时,因每一个新的刺激到来时由前一次刺激引起的单收缩过程(包括舒张期)已经结束,于是每次刺激都引起一次独立的单收缩;当刺激频率增加到某一限度时,后来的刺激有可能在前一次收缩的舒张期结束前即到达肌肉,于是肌肉在自身尚处于一定程度的缩短或张力存在的基础上进行新的收缩,发生了所谓收缩过程的复合,这样连续进行下去,肌肉就表现为不完全强直收缩,其特点是每次新的收缩都出现在前次收缩的舒张期过程中,在描记曲线上形成锯齿形;如果刺激频率继续增加,那么肌肉就有可能在前一次收缩的收缩期结束以前或在收缩期的顶点开始新的收缩,于是各次收缩的张力或长度变化可以融合而叠加起来,使描记曲线上的锯齿形消失,这就是完全强直收缩。
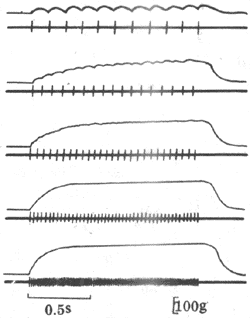
图2-28 不同频率的连续刺激对骨骼肌收缩的影响
每组曲线中,上方曲线是肌肉等长收缩的记录,下方曲线是肌肉动作电位的记录,
注意由上而下当刺激频率依次增加时,机械收缩可出现逐渐融合,
表现不完全和完全强直收缩,但动作电位始终彼此分离,不发生融合和叠加
由于正常体内由运动神经传到骨骼肌的兴奋冲动都是快速连续的,体内骨骼肌收缩几乎都属于完全强直收缩,只不过强直收缩的持续时间可长可短。强直收缩显然可以产生更大的收缩效果,例如,强直收缩所能产生的最大张力可达单收缩的4倍左右。这是因为肌肉在只接受一次刺激时,释放到肌浆中的Ca2+很快被肌浆网上的Ca2+泵回收入肌浆网,而连续刺激可使肌浆中的Ca2+维持在一个饱和的高浓度水平。不同肌肉单收缩的持续时间不同,因而能引起肌肉出现完全强直收缩的最低临界频率在不同肌肉也不同,例如,单收缩快速的眼球内直肌需要每秒约350次的高频刺激才能产生完全强直收缩,而收缩缓慢的比目鱼肌只需每秒约30次的频率就够了。但不论在不完全强直收缩或完全强直收缩,伴随每次刺激出现的肌肉动作电位只出现频率加快,却始终各自分离而不会发生融合或总和;这是由于肌肉的动作电位只持续1~2ms,当刺激频率加速到下一次刺激落于前一次刺激引进起的动作电位持续期间时,组织又正好处于兴奋的绝对不应期,这时新的刺激将无效,既不能引起新的动作电位产生,也不引起新的收缩。
五、平滑肌的结构和生理特性
平滑肌广泛分布于人体消化道、呼吸道以及血管和泌尿、生殖等系统;它和骨骼肌不同,不是每条肌纤维(即肌细胞)的两端都通过肌腱同骨骼相连;平滑肌细胞互相连接,形成管状结构或中空器官;在功能上可以通过缩短和产生张力使器官发生运动和变形,也可产生连续收缩或紧张性收缩,使器官对抗所加负荷而保持原有的形状,前者如胃和肠,后者如动脉血管、括约肌等。此外,也不能像在骨骼肌和心肌那样,把分布在不同器官的平滑肌看作具有相同功能特性和调节机制的组织,例如有些器官的平滑具有和心脏一样的自动节律性,有些则像骨骼肌那样,只有在支配它的神经纤维有神经冲动到来时才出现收缩,而在这两个极端之间,还存在着各种的过渡形式,致使平滑肌的分类困难。
(一)平滑肌的微细结构和收缩机制
平滑肌虽然也具有同骨骼肌类似的肌丝结构,但由于它们不存在像骨骼肌那样平行而有序的排列(平滑肌的肌丝有它自己的“有序的”排列),图2-29是根据最近观察提出的平滑肌细胞内部假想结构图,它的特点是细胞内部存在一个细胞骨架,包含一些卵圆形的称为致密体的结构,它们也间隔地出现于细胞膜的内侧,称为致密区,并且后者与相邻细胞的类似结构相对,而且两层细胞膜也在此处连结甚紧,因而共同组成了一种机械性耦联,藉以完成细胞间张力的传递;细胞间也存在别的连接形式,如缝隙连接,它们可以实现细胞间的电耦联和化学耦联。在致密体和致密区中发现有同骨骼肌Z带中类似的蛋白成分,故认为这两种结构可能是与细肌丝连接的部位。另外,在致密体和致密区之间还有一种直径介于粗、细肌丝之间的丝状物存在,它们是一种称为结蛋白(desmin)的聚合体。这样由丝状物联结起来的致密体和膜内侧的致密区就形成了完整的细胞内构架。
平滑肌细胞中的细肌丝有同骨骼肌类似的分子结构,但不含肌钙蛋白;同一体积的平滑肌所含肌纤蛋白的量是骨骼肌的2倍,推测平滑肌肌浆中有大量细肌丝存在,它们的排列大致与细胞长轴平行。与此相反,胞浆中肌凝蛋白的量却只有骨骼肌的1/4。估计连接在致密体上的3~5根细肌丝会被较少数目粗肌丝包绕,形成相互交错式的排列,这可能就是类似于骨骼肌中肌小节的功能单位。
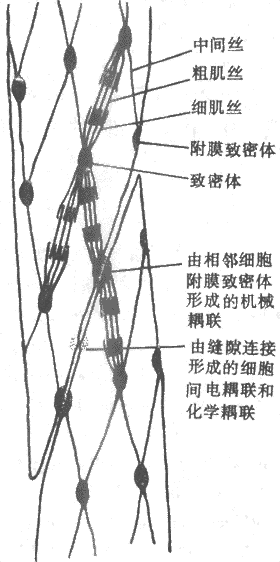
图2-29平骨肌内部结构和相互关系模式图
一般平滑肌细胞呈梭形,直径2~5μm;其长度可变性很大,大约长度为400μm时是产生张力的最适长度。它们没有骨骼肌(和心肌)那样发达的肌管系统。肌细胞膜只有一些纵向排列的袋状凹入,但其功能尚不清楚,不过这使得细胞膜表面积和细胞体积之比更为加大,因此和肌丝靠近的不是横管或肌浆网系统,而是肌膜。细胞被激活时,细胞外Ca2+进入膜内,但平滑肌细胞中靠近膜的肌浆网也构成了细胞内Ca2+贮存库。一些兴奋性递质、激素或药物同肌膜受体结合时,通过G-蛋白在胞浆中产生第二信使,引起Ca2+库中的Ca2+释出。因平滑肌的细肌丝中不存在肌钙蛋白,因而Ca2+引起平滑肌细胞中粗、细肌丝相互滑行的横桥循环的机制与骨骼肌不同。目前认为,横桥的激活开始于它的磷酸化,而这又依赖一称为肌凝蛋白激酶的活化;其过程是Ca2+先结合于胞浆中一种称为钙调蛋白(calmodulin)的特殊蛋白质,后者结合4个Ca2+之后才使肌凝蛋白激酶活化,使ATP分解,由此产生的磷酸基结合于横桥并使横桥处于高自由状态。比起平滑肌来,平滑肌横桥激活的机制需要较长的时间,这和平滑肌收缩的缓慢相一致。
(二)平滑肌在功能上的分类
尽管体内各器官所含平滑肌在功能特性上判别很大,但一般可分为两大类:一类称为多单位(multi-unit)平滑肌,其中所含各平滑肌细胞在活动时各自独立,类似骨骼肌细胞,如竖毛肌、虹膜肌、瞬膜肌(猫)、以及大血管平滑肌等,它们各细胞的活动受外来神经支配或受扩散到各细胞的激素的影响;另一类称为单位(single-unit)平滑肌,类似心肌组织,其中各细胞通过细胞间的电耦联而可以进行同步性活动,这类平滑肌大都具有自律性,在没有外来神经支配时也可进行近于正常的收缩活动(由于起搏细胞的自律性和内在神经丛的作用),以胃肠、子宫、输尿管平滑肌为代表。还有一些平滑肌兼有两方面的特点,很难归入哪一类,如小动脉和小静脉平滑肌一般认为属于多单位平滑肌,但又有自律性;膀胱平滑肌没有自律性,但在遇到牵拉时可作为一个整体起反应,故也列入单位平滑肌。
(三)平滑肌活动的控制和调节
和平滑肌本身的特性具有多样性一样,它们活动所受的调控也是多种多样的,不象骨骼肌那样单纯。大多数平滑肌接受神经支配,包括来自自主神经系统的外来神经支配,其中除小动脉一般只接受交感系统一种外来神经支配外,其他器官的平滑肌通常接受交感和副交感两种神经支配。平滑肌组织、特别是消化管平滑肌肌层中还有内在神经丛存在,后者接受外来神经的影响,但其中还发现有局部传入性神经元,可以引起各种反射。平滑肌的神经-肌接头有些类似骨骼肌,但不具有后者那样特殊结构形式。支配平滑肌的外来神经纤维在进入靶组织时多次分支,分支上每隔一定距离出现一个膨大,呈念珠状,称为曲张体,其中含有分泌囊泡,它们在神经冲动到达时可以释放其中递质或其他神经活性物质;每个曲张体和靶细胞的距离亦不固定,平均约为80~100nm,这说明由神经末梢释放出来的递质分子要扩散较远距离才能达到靶细胞,而靶细胞和神经末梢的关系也不可能是固定的;凡是递质分子可以到达而又具有该递质受体的平滑肌细胞,都可能接受外来神经的影响。
平滑肌细胞约保持-55~-60mV的静息电位,产生机制和骨骼肌类似。单位平滑肌细胞有产生动作电位的能力,而且通过细胞间通道可使相邻细胞也产生动作电位。
参考资料
· 乔健天,关于兴奋膜的一些基本概念和新进展.生理科学进展1980;11:193~200
· 董政,朱培闳.肌醇磷脂信使系统调控骨骼肌兴奋收缩耦联.生理科学进展1994;25:121~125
· BerneRM,Levy MN.Physiology 3rd ed,CV Mosby Co,StLouis,1993
· WrightFM.The intestinal Na/glucose cotransporter .Ann Rev Physiol 1993;55:575~589
· ThorensR.Facilitated glucose transporters in epithelial cells.Ann Rev Physiol1993;55:591~608
· Simon.MI,Strathman MP,Gautam N.Diversity of G-protein in signaltransduction .Science 1991;252:802
· FantlWJ,Johnson DE,Williams LT.Signaling by receptor tyrosine kinases.Ann RevBiochem 1993;62:453~481
· StraderC,Fang TM,Dixon RAT.Structure and function of G-protein-coupled receptors.AnnRev Biochem 1994;63:101~132
· ClaphamD,Found M,Rochester MN.Direct G-protein activation of ion channel?Ann RevNeurosci 1994;17:441~464
· HodgkinAL.The ionic basis of nervous conduction.Science 1964;145:1148~1153
· BezanillaF,Steffani E.Voltage-dependent gating of ionic channels .Ann Rev Biophy andBiomol Structure 1994;23:819~846
· NeherE.Ion channels for communication between and within cells.Neuron 1992;8:605~612
· SakmannB.Elementary steps in synaptic transmission revealed by currents through singleion channels .Neuron 1992;8:613~629
· FrenchAS.Mechanotransduction.Ann Rev Physiol 1992;54:135~152
· ShengM,Greenberg MF.The regulation and function of c-fos and other immediate earlygenes in the nervous system .Neuron 1990;4:477~485
· FrancisArmstrong C,Jorgensen AO.Structure and development of E-C coupling units inskeletal muscle .Ann Rev Physiol 1994;56:509~534
· MottaPM.Ultrastructure of Smooth Muscle .Kluwer Academic Publishers.Lancaster,England,1990
· GalziJL,Revah F,Bessis A,Changeux JP.Functional architecture of the nicotinicacetylcholine receptor:from electric organ to brain .Ann Rev Pharmacol1991;31:37~72
· CatterallWA.Structure and function of voltage-gated ion channels.TINS 1993;16:500
· Huxley HE.The mechanism of muscle contraction .Science 1969;164:1355~1366